Cancer de prostată
Cancerul de prostata
- Simptome urinare
- Disfuncții erectile
- Ejaculare dureroasă
- Scădere în greutate
- Durere de spate, șolduri sau pelvis ce nu dispare
- Stări de oboseală, amețeli sau paloare
- Slăbiciune, amorțeală sau edeme la nivelul picioarelor
- Dureri osoase persistente
* la cererea medicului oncolog
** pasii exacti de urmati de la momentul diagnosticului se decid NUMAI impreuna cu medicul oncolog, investigatiile suplimentare se fac doar la cererea acestuia
*** primul pas este sa mergeti catre medicul de familie pentru consult si recomandari
Prostata este o glandă mică din pelvis și face parte din sistemul reproducător masculin, fiind un organ musculo-glandular, alcătuit din parenchim glandular și stroma fibromusculară. Dimensiunea prostatei se poate schimba pe măsură ce bărbatul îmbătrânește. La bărbații mai tineri, este de dimensiunea unei nuci/castane, însă pe măsură ce bărbatul îmbătrânește, se poate mari. Aceasta este situată sub vezică, anterior de rect și înconjoară partea superioară a uretrei, tubul care transportă urina și lichidul seminal din corp prin penis. în spatele prostatei se află veziculele seminale, mici glande ce produc o mare parte a lichidului seminal.
Cancerul de prostată apare atunci când celulele din glanda prostatică încep să crească necontrolat.
Din punct de vedere epidemiologic, incidența cancerului de prostată este în creștere continuă, fiind a II-a cauza de cancer (după cancerul de sân) și a IV-a cauza de deces prin cancer (după cancerul de plămân, sân și colorectal). La nivel global, ocupă locul 4 ca incidență și locul 9 ca mortalitate. Această diferență între incidență și mortalitate este determinată de eficacitatea metodelor de tratament de care dispunem.
În general, afecțiunea se dezvoltă lent și afectează în special bărbații cu vârsta>50 ani. Cu cât crește mai mult vârsta cu atât crește și șansa de a diagnostica un cancer de prostată. De aceea, rata cancerului de prostată este în general, mai mare în părțile lumii cu speranță de viață mai mare. 1 din 8 bărbați sunt predispuși de-a lungul vieții să dezvolte cancer de prostată.
Din fericire, aproximativ 85% din pacienți se află în stadii incipiente (cancerul nu depășește capsula prostatică). Cu cât cancerul este depistat într-o fază mai incipientă, cu atât șansele de vindecare sunt mai mari.
- Adenocarcinomul de prostată acinar sau adenocarcinomul acinar prostatic (se dezvoltă la la nivelul celulelor glandei care acoperă glanda prostatică)
- Adenocarcinom de prostată ductal (se dezvolta la nivelul celulelor care acoperă tubii prostatei) - crește și se răspândește mai rapid decât forma acinară.
În afară de acestea, mai există și alte tipuri de cancer de prostată, însă mult mai rare:
- Carcinoame cu celule tranziționale - urotelial (se dezvoltă în celulele care acoperă uretra - tubul ce transportă urina în exteriorul corpului)
- Carcinoame cu celule mici (format din celule mici rotunde - un tip de cancer neuroendocrin)
- Tumori neuroendocrine (altele decât carcinoamele cu celule mici)
- Sarcoame
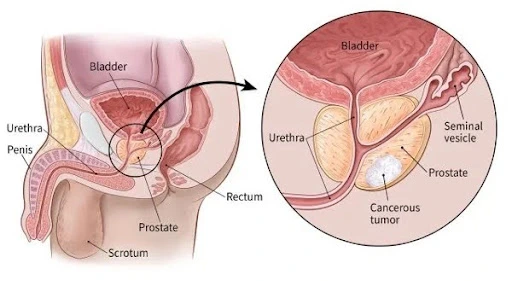
Deși cauzele cancerului de prostată sunt în mare parte necunoscute, anumiți factori pot crește riscul de a dezvolta cancer de prostată.
Unul dintre acești factori pot fi:
- Mutațiile genetice progresive din celulele prostatice, ce le determină să se dividă mult mai rapid și necontrolat, putând astfel să formeze o tumoră cu potențial de extindere locală și la distanță dacă nu este tratată. Doar în aproximativ 9% din cazuri cancerul este ereditar (agregare familiala-2,3 rude cu cancer de prostată diagnosticat sub vârsta de 55 de ani - unele din genele incriminate fiind BRCA1 si BRCA2). Riscul de a dezvolta cancer de prostată este cu mult mai mare la pacienții care au o rudă de gradul I diagnosticată cu cancer de prostată (tata,frate,fiu), sau la cei ce au rude diagnosticate cu cancer de sân. Riscul de a dezvolta crește de 2 ori la cei cu o rudă, de 5 ori la cei cu 2 rude și de până la 7 ori la cei cu o rudă diagnosticată înainte de 50 de ani. De asemenea s-a dovedit că cei cu mutații ale genelor Sd Lynch (MLH1,MSH2,MSH6) sunt mai predispuși să facă cancer de prostată față de restul populației.
- Vârsta -riscul de a dezvolta cancer crește odată cu înaintarea în vârstă, fiind mai frecvent diagnosticat după vârsta de 50 de ani. Aproximativ 6 din 10 bărbați sunt diagnosticați peste vârsta de 65 de ani.
- Rasa - din motive încă necunoscute, cancerul de prostată este mai frecvent la persoanele de culoare față de cei de alte rase.
- Alimentația- o alimentație haotică cu aport crescut în grăsimi saturate, precum și obezitatea cresc riscul de a dezvolta cancer de prostată.
- Hormonii - testosteronul este principalul hormon masculin ce ajută organismul să se dezvolte și să mențină funcția sexuală. Pacienții care beneficiază de tratamente cu testosteron, au risc mai mare de a dezvolta cancer de prostata întrucât un nivel crescut de testosteron duce și la o creștere a prostatei.
- Neoplazia intraepitelială prostatică (PIN)
- PIN de grad scăzut: celulele prostatice par aproape normale.
- PIN de grad înalt: celulele prostatice arată mai anormal.
PIN-ul de grad scăzut nu este considerat ca fiind precursor al cancerului de prostata față de PIN-ul de grad înalt care este văzut ca un precursor.
Pacienții cu PIN de grad înalt depistat la biopsia de prostată au un risc mai mare ca în timp să dezvolte cancerul de prostată.
Această neoplazie intraepitelială prostatică la unii pacienți poate să se dezvolte încă de la vârsta de 20 de ani, însă nu e obligatoriu ca aceștia să dezvolte cancer de prostată de-a lungul vieții.
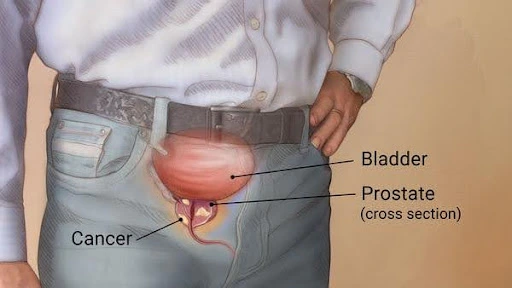
Alimentația : Dieta bogată în grăsimi saturate, în special din surse animale, a fost asociată cu un risc crescut de cancer de prostată. Consumul excesiv de carne roșie și produse lactate grase poate juca un rol în acest proces.Obiceiurile alimentare : Un aport redus de fructe și legume poate fi asociat cu un risc mai mare de cancer de prostată. În schimb, consumul de alimente bogate în antioxidanți și substanțe nutritive poate oferi o protecție.Sedentarismul : Lipsa activității fizice regulate poate fi asociată cu un risc crescut de cancer de prostată. Exercițiile regulate pot ajuta la menținerea unei greutăți corporale sănătoase și pot avea efecte benefice asupra sistemului imunitar.Fumatul : Fumatul poate crește riscul de cancer de prostată, iar renunțarea la fumat poate avea beneficii semnificative pentru sănătate.Consumul de alcool : Consumul excesiv de alcool a fost asociat cu un risc crescut de cancer de prostată. Limitarea sau evitarea consumului de alcool poate contribui la reducerea riscului.Expunerea la substanțe chimice : Anumite substanțe chimice sau toxice prezente în mediul de lucru sau în mediul înconjurător pot contribui la dezvoltarea cancerului de prostată.Radiații : Expunerea la radiații ionizante, fie din surse medicale, fie din mediu, poate crește riscul de cancer, inclusiv de cancer de prostată.Poluarea aerului : Anumite niveluri ridicate de poluare a aerului au fost asociate cu un risc crescut de cancer de prostată.Istoricul familial și factorii genetici : Dacă un membru al familiei a avut cancer de prostată, riscul poate crește. Anumite mutații genetice pot, de asemenea, contribui la predispoziția pentru cancerul de prostată.Stresul și calitatea somnului : Stresul cronic și lipsa somnului pot afecta sistemul imunitar și pot juca un rol în dezvoltarea cancerului, inclusiv a celui de prostată.
Majoritatea cancerelor de prostată sunt depistate precoce prin screening. Deși în stadiile incipiente nu provoacă simptome, în stadiile mai avansate pot apărea simptome.
- Simptome urinare: Jet urinar mai lent/slab sau întrerupt, urinari frecvente - în special noaptea(nicturie), nevoia imperioasă de urinare, dificultăți în golirea completă a vezicii urinare, arsuri/dureri la urinare(disurie), sânge în urina(hematurie) sau prezența sângelui în spermă, incontinență urinară.
- Disfuncții erectile
- Ejaculare dureroasă
- Scădere în greutate
- Durere de spate, șolduri sau pelvis ce nu dispare
- Stări de oboseală, amețeli sau paloare (cauzate de anemie)
- Slăbiciune, amorțeală sau edeme la nivelul picioarelor
- Dureri osoase persistente
Aceste simptome nu sunt specifice cancerului de prostata, putând fi și simptome cauzate de afecțiuni benigne.
În faza terminală a cancerului de prostată, pacienții pot experimenta:
- Durere intensă
- Oboseală extremă
- Pierderea în greutate
- Dificultăți în respirație
- Probleme digestive
- Probleme urinare
- Depresie și anxietate
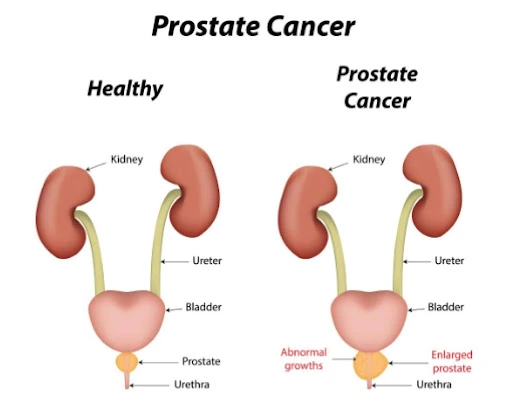
Screening-ul în cancerul de prostata este încă un subiect extrem de controversat întrucât prezintă atât potențiale avantaje (diagnosticarea într-un stadiu incipient, reducând riscul de diseminare și metastazare) precum și dezavantaje (stresul psihologic determinat de depistarea și tratarea inadecvată a unei astfel de afecțiuni în cazul unor pacienți în varsta la care șansele de a produce probleme serioase sunt reduse).
Majoritatea organizațiilor medicale încurajează bărbații de peste 50 de ani să discute cu medicii lor despre avantajele și dezavantajele acestui screening pe baza factorilor de risc pe care îi au. Cu cât există mai mulți factori de risc (vârsta, rasa, Sd Lynch, cancer de prostată sau sân în familie, prezența genelor BRCA1, BRCA2) cu atât această discuție ar trebui să se înceapă mai din timp.
Acest screening se poate realiza cu ajutorul testelor de sânge prin dozarea biomarkerului PSA (prostate-specific antigen) și prin examinare clinică- tușeu rectal-DRE (digital rectal examination). Aceste teste sunt folosite pentru a căuta posibile semne de cancer de prostată și pentru a îl diagnostica în stadii incipiente, însă niciunul din ele nu poate pune cu certitudine diagnosticul și în cazul în care ies modificate/anormale necesită în continuare alte investigații complementare.
Antigenul specific prostatic (PSA) este o proteină produsă de celulele glandei prostatice (atât celulele normale, cât și celulele canceroase). PSA-ul se găsește mai ales în spermă, dar o cantitate mică se găsește și în sânge. Riscul de a avea cancer de prostata crește odată cu creșterea nivelului de PSA. În general majoritatea medicilor iau în considerare investigațiile suplimentare în momentul când PSA-ul depășește valoarea de 4ng/ml, însă nu există nici o certitudine că la cei cu valori sub 4 ng/ml în cazul în care s-ar face o biopsie aceștia nu ar avea cancer.
Bărbații cu nivelul PSA-ului între 4 și 10 (numit adesea „interval limită”) au aproximativ 1 din 4 șanse de a avea cancer de prostată. Dacă PSA-ul este mai mare de 10, șansa de a avea cancer de prostată este de peste 50%. Cu toate acestea, un PSA mărit nu poate pune cu certitudine acest diagnostic, întrucât există o serie de factori ce pot crește aceste valori ale PSA-ului.
Dintre acești factori ce pot duce la creșterea valorilor PSA-ului putem enumera:
- Hiperplazia benignă de prostată (HBP), o mărire a prostatei ce se produce odată cu înaintarea în vârstă.
Vârsta înaintată : nivelurile de PSA cresc lent în mod normal odată cu înaintarea în vârstă fără a exista o anomalie a prostatei.Prostatită : infecție sau inflamație a glandei prostatei, ce poate determina creșterea nivelului de PSA.Ejacularea : poate duce la creșterea pentru o perioadă scurtă de timp a PSA-ului, de aceea majoritatea medicilor sugerează ca bărbații să se abțină de la ejaculare timp de o zi sau două înainte de testare.Mersul pe bicicletă: : Unele studii au sugerat că ciclismul poate crește nivelul PSA pentru o perioadă scurtă de timp (posibil pentru că scaunul pune presiune asupra prostatei).Anumite proceduri urologice : biopsia de prostată sau cistoscopia, pot crește nivelul PSA-ului pentru o perioadă scurtă de timp. De asemenea, unele studii au arătat că inclusiv tușeul rectal (DRE) ar putea duce la creșterea ușoară a PSA-ului. Totuși, dacă în cadrul unei vizite la doctor se face atât testul PSA, cât și DRE, atunci se recomandă prima dată să se recolteze PSA-ul.Anumite medicamente : medicamente pe baza de hormoni masculini precum testosteronul (sau alte medicamente care cresc nivelul de testosteron) pot determina o creștere de PSA.
De asemenea exista o serie de factori ce pot duce la scăderea valorilor PSA-ului.
- Inhibitori de 5-alfa reductaza: Anumite medicamente utilizate pentru a trata BPH sau simptome urinare, cum ar fi finasterida sau dutasterida,pot scădea nivelul PSA.
- Suplimentele alimentare ar putea masca un nivel ridicat de PSA.
- Anumite medicamente: utilizarea pe termen lung a anumitor medicamente, cum ar fi aspirina, statinele (medicamente care scad colesterolul) și diureticele tiazidice(cum ar fi hidroclorotiazida) ar putea scădea nivelul PSA.
În concluzie, screening-ul pare să indice totuși o tendință de reducere a mortalității și tinde să fie totuși recomandat persoanelor peste vârsta de 50 de ani și cu factori de risc prezenți în cazul în care aceștia vor să obțină un diagnostic cât mai precoce și sunt dispuși să își asume investigațiile invazive excesive.
În cazul în care se ridica suspiciunea de cancer de prostată în urma rezultatelor screening-ului sau a simptomelor, pacientul este îndrumat către un urolog.
Anamneza, examenele clinice, paraclinice și imagistice pot pune diagnosticul, însă diagnosticul de certitudine se poate pune doar în urma unei biopsii de prostată.
La un pacient cu PSA crescut și/sau simptome, se efectuează examenul clinic - tușeu rectal(DRE)-(o examinare clasică pentru a aprecia dimensiunea, consistența, limitele și sensibilitatea prostatei) și în continuare se poate recomanda o ecografie transrectală (este introdusă o sondă mică în rect și cu ajutorul unor unde sonore, se poate reconstitui imaginea prostatei), RMN pelvin cu sc/RMN multiparametric specific prostatei și biopsie prostatica.
PI-RADS, sau Prostate Imaging Reporting and Data System, este un sistem standardizat de clasificare utilizat în imagistica medicală pentru a evalua rezultatele imaginilor rezonanței magnetice (RMN) ale prostatei. Scopul PI-RADS este să ajute la standardizarea interpretării imaginilor și să ofere informații despre probabilitatea prezenței cancerului de prostată.
Scorul PI-RADS atribuie un scor între 1 și 5, unde:
PI-RADS 1 : Foarte scăzută probabilitate de cancer.PI-RADS 2 : Probabilitate scăzută de cancer.PI-RADS 3 : Probabilitate intermediară de cancer.PI-RADS 4 : Probabilitate moderată de cancer.PI-RADS 5 : Probabilitate mare de cancer
Biopsia prostatică se poate efectua prin 3 tehnici de abordare: rectala - cea mai frecventă (cu ajutorul ecografiei transrectale), perineală și uretrala (cu ajutorul unui cistoscop introdus în uretră).
Fragmentele de țesut prostatic recoltate în urma biopsiei sunt analizate într-un laborator pentru a verifica dacă conțin celule canceroase, și astfel se calculează scorul Gleason în funcție de cele 5 etape de dezvoltare ale celulelor tumorale, pe măsură ce se modifică pentru a forma tumori. Cu cât gradul este mai mare, cu atât celulele sunt mai anormale și au mai multe șanse să se dezvolte și să se răspândească mai rapid. Aproape toate cancerele sunt de gradul 3 sau mai mare; clasele 1 și 2 nu sunt folosite des.
Deoarece cancerele de prostată au adesea zone cu grade diferite, un grad este atribuit celor 2 zone care alcătuiesc cea mai mare parte a cancerului. Aceste 2 note sunt adăugate pentru a obține scorul Gleason (numit și suma Gleason). Primul număr atribuit este gradul care este cel mai frecvent în tumoră. Deși cel mai adesea, scorul Gleason se bazează pe cele 2 zone care alcătuiesc cea mai mare parte a cancerului, există unele excepții când o probă de biopsie are fie o mulțime de cancer de grad înalt, fie există 3 grade, inclusiv cancer de grad înalt. În aceste cazuri, modul în care este determinat scorul Gleason este modificat pentru a reflecta natura agresivă (cu creștere rapidă) a cancerului.
În teorie, scorul Gleason poate fi între 2 și 10, dar scorurile sub 6 sunt rareori folosite
Pe baza scorului Gleason, cancerele de prostată sunt adesea împărțite în 3 grupuri:
- Gleason <=6 -cancer bine diferențiat/grad scăzut
- Gleason 7 -cancer moderat diferențiat/grad intermediar.
- Gleason 8-10 -cancer slab diferențiat/grad înalt.
În ultimii ani, medicii au ajuns la concluzia că scorul Gleason nu este suficient pentru a descrie gradul cancerului și au dezvoltat grupuri de grad, care variază de la 1 (cel mai probabil să crească și să se răspândească lent) la 5 (cel mai probabil să crească și să se răspândească rapid):
- Grupa de grad 1 = Gleason 6 (sau mai puțin)
- Grupa de nota 2 = Gleason 3+4=7
- Grupa de nota 3 = Gleason 4+3=7
- Grupa de nota 4 = Gleason 8
- Grupa de nota 5 = Gleason 9-10
Pe lângă gradul cancerului, anatomopatologul ne mai poate oferi informații în buletinul histopatologic și despre numărul de probe prelevate prin biopsie care conțin cancer (de exemplu, „7 din 12”) și procentul de cancer în fiecare dintre nuclee indiferent dacă cancerul este pe o parte (stânga sau dreaptă) a prostatei sau pe ambele părți (bilateral).
Stadializarea este o modalitate de a descrie localizarea cancerului și răspândirea acestuia. Există 2 tipuri de stadializare: CLINICĂ (se bazează pe rezultatul testelor efectuate înainte de intervenția chirurgicală- biopsie, CT, RMN, scintigrafie) și stadializarea PATOLOGICĂ (se bazează pe rezultatele obținute în urma analizei țesutului prostatic recoltat în timpul intervenției chirurgicale). Investigațiile imagistice se recomandă în funcție de rezultatul biopsie (scorul GLEASON) și PSA. Cu cât Scorul Gleason și PSA-ul este mai mare, cu atât este nevoie de mai multe investigații imagistice pentru a stabili cât de mult s-a extins cancerul. Sistemul de Stadializarea pentru cancerul de prostată este sistemul TNM AJCC (American Joint Committee on Cancer), care a fost actualizat cel mai recent în 2018.
Sistemul TNM pentru cancerul de prostată se bazează pe 5 informații cheie:
- T-Extinderea tumorii principale (primare)
- N-Dacă boala s-a răspândit la ganglionii limfatici din apropiere
- M-Dacă boala s-a răspândit (metastazat) în alte părți ale corpului
- Nivelul PSA la momentul diagnosticului
- Grupul de grad (pe baza scorului Gleason)-care stabilește ritmul de creștere și răspândire a cancerului.
- TX: tumora primară nu poate fi evaluată;
- T0: nu există dovezi ale unei tumori în prostată;
- T1: tumora nu poate fi simțită în timpul unei examen fizic și nu este observată în timpul testelor imagistice, dar sunt depistate celule canceroase în țesuturile analizate;
- T1a: tumora este în 5% sau mai puțin din țesutul de prostată prelevat în timpul intervenției chirurgicale;
- T1b: tumora este în mai mult de 5% din țesutul prostatic prelevat în timpul intervenției chirurgicale;
- T1c: tumora se găsește în timpul unei biopsii cu ac;
- T2: tumora se găsește numai în prostată, nu în alte părți ale corpului;
- T2a: tumora implică o jumătate de lob al prostatei;
- T2b: tumora implică mai mult de o jumătate de lob al prostatei, dar nu ambii;
- T2c: tumora a crescut în ambii lobi ai prostatei;
- T3: tumora a trecut prin capsula prostatei și în țesutul din afara prostatei;
- T3a: tumora a depasit capsula, fie pe o parte, fie pe ambele părți ale prostatei, sau s-a extins la vezică;
- T3b: tumora a crescut în veziculele seminale, tubul (tuburile) care transportă materialul seminal;
- T4: tumora este fixată sau s-a dezvoltat în structurile din apropiere, altele decât veziculele seminale, cum ar fi sfincterul extern, rectul sau peretele pelvin.
- NX: ganglionii limfatici regionali nu pot fi evaluați;
- N0: cancerul nu s-a răspândit la ganglionii limfatici regionali;
- N1: cancerul s-a răspândit la ganglionii limfatici regionali.
- MX: metastazele la distanță nu pot fi evaluate;
- M0: boala nu a metastazat;
- M1: există metastaze îndepărtate;
- M1a: cancerul s-a răspândit la noduli limfatici îndepărtați;
- M1b: cancerul s-a răspândit în oase;
- M1c: cancerul s-a răspândit în altă regiune a corpului, cu sau fără răspândire la nivelul osului.
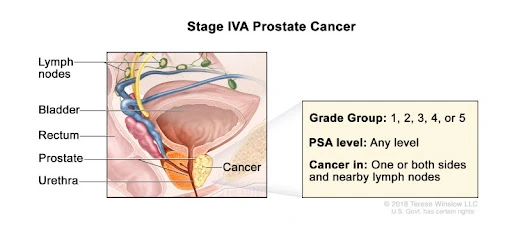
În funcție de categoria T, nivelul inițial al PSA-ului, grupul de grad și scorul Gleason, pentru a stabili opțiunile de tratament optime pentru pacienți, medicii le împart în grupuri de risc .
Astfel, există 4 grupuri:
- Grup cu risc foarte scăzut
- Grup cu risc scăzut
cT2a, grup grad 1, Gleason<=6, PSA<10 - Grup cu risc intermediar favorabil/ nefavorabil
T2b/T2c / Gleason7/grup grad 2/3 si sau PSA=10-20ng/ml - Grup cu risc crescut
cT3a/ grup grade 4/5/ Gleason 8-10 /PSA>20ng/ml - Grup cu risc foarte crescut
cT3b/cT4, grup grad 5/ Gleason9/10 sau au 2-3 caracteristici găsite în grupul cu risc crescut.
Adenocarcinom acinar prostatic scor Gleason 7:
-
Adenocarcinom: Tipul cel mai comun de cancer de prostată, care se dezvoltă din celulele glandulare ale prostatei.
-
Acinar: Se referă la structura glandulară a prostatei.
-
Scor Gleason 7: Scorul Gleason este o metodă de evaluare a gradului de malignitate a cancerului de prostată. Scorul poate varia de la 2 la 10, cu 2 indicând cel mai puțin agresiv cancer și 10 cel mai agresiv. Un scor Gleason 7 indică un cancer moderat de prostată, fiind alcătuit din două zone de cancer cu grad de diferențiere diferit, fiecare cu o notație de la 3 la 4.
Adenocarcinom prostatic acinar scor Gleason 9:
Aici avem același tip de cancer, dar cu un scor Gleason mai mare. Un scor Gleason 9 indică un cancer de prostată mai agresiv, cu celule mai puțin diferențiate și un risc mai mare de răspândire rapidă.
Adenocarcinom acinar prostatic scor Gleason 7 3 4:
Această descriere specifică gradul de diferențiere al celulelor tumorale. Scorul Gleason 7 3 4 indică faptul că două dintre cele trei componente ale cancerului au un grad de diferențiere de 3 și una are un grad de diferențiere de 4, ceea ce poate afecta prognosticul și opțiunile de tratament.
Durata de supraviețuire pentru cancerul de prostată variază considerabil în funcție de mai mulți factori, inclusiv stadiul la momentul diagnosticului, gradul de agresivitate al cancerului, vârsta și starea generală de sănătate a pacientului, precum și modul în care cancerul răspunde la tratament.
Stadiul 4 al cancerului de prostată se referă la un stadiu avansat, în care cancerul s-a răspândit la distanță de prostată către alte organe sau țesuturi din corp. Prognosticul în cazul cancerului de prostată în stadiul 4 poate varia considerabil în funcție de mai mulți factori, cum ar fi gradul de agresivitate al cancerului, răspândirea exactă a acestuia, starea generală de sănătate a pacientului și răspunsul la tratament.
În general, prognosticul pentru cancerul de prostată în stadiul 4 poate fi rezervat, iar tratamentul se axează, în principal, pe gestionarea simptomelor și menținerea calității vieții.
Pacienții sunt tratați individual, iar opțiunile de tratament depind de mai mulți factori, cum ar fi: starea generală de sănătate (comorbiditățile asociate), vârsta și speranța de viață, grupul de risc, precum și potențialele beneficii sau efecte secundare ale tratamentului.
Strategiile terapeutice presupun mai multe scheme unice sau combinate și constă fie în supraveghere activă, fie în tratament local sau tratament sistemic.
Tratamentul local (chirurgia, radioterapia, HIFU și crioablatia)-se utilizează de obicei pentru pacienții cu boala localizată cu scopul vindecării.
Tratamentul sistemic (Hormonoterapia, chimioterapia, imunoterapia, terapia cu radioizotopi și tratamentul pentru metastazele osoase)-se utilizează pentru pacienții cu boală avansată în care tratamentul local nu poate acoperi extensia bolii.
Supravegherea activă- poate fi o opțiune în unele cazuri în care efectele secundare depășesc beneficiile (pacienți cu comorbidități multiple, vârstă înaintată, stare generală care să îngreuneze tratamentul) sau în cazurile incipiente de cancer (PSA<10, Gleason<7, stadiul T1/T2a, un timp de dedublare a PSA-ului mai lent).
- Chirurgia este cea mai frecventă metodă de tratament local. Poate fi realizată clasic -prostatectomie radicală deschisă sau laparoscopic -prostatectomie laparoscopica. Operația constă în îndepărtarea în totalitate a prostatei (prostatectomie radicală), îndepărtarea unor țesuturi înconjurătoare și a câtorva ganglioni limfatici (limfadenectomie pelvină).O altă abordare include și rezecția transuretrală de prostată(TUR-P) -eliminarea unei porțiuni de țesut prostatic cu ajutorul unui rezectoscop prin uretră, metoda utilizată pentru tratarea hipertrofiei de prostata sau atunci când se dorește ameliorarea simptomelor cauzate de cancer.
Riscurile prostatectomiei sunt similare riscurilor oricărei intervenții chirurgicale:
- reacții adverse la anestezie
- sângerări la nivelul plăgii operatorii
- formarea de cheaguri de sânge în picioare sau plămâni
- afectarea organelor învecinate
- infecții la nivelul plăgii operatorii
- incontinența urinară
- disfuncții erectile (impotență)
- infertilitate
- limfedem
- modificări ale dimensiunilor penisului (micșorarea)
- hernie inghinală
- modificări ale orgasmului (scăderea în intensitate sau chiar dispariția).
După operația de prostată, nivelul PSA (antigenul specific prostatic) ar trebui să scadă semnificativ sau să devină nedetectabil în sânge. Este important să înțelegem că după o intervenție chirurgicală, nivelul PSA poate fi măsurat, dar există o perioadă de recuperare în care valorile PSA pot varia în mod natural. În general, valoarea PSA după operația de prostată ar trebui să fie nedetectabilă sau foarte scăzută în sânge, deoarece sursa principală a PSA, adică prostata, a fost eliminată.
Speranța de viață după o operație de prostată depinde de mai mulți factori, inclusiv stadiul cancerului de prostată, gradul de agresivitate al tumorii, vârsta pacientului, starea generală de sănătate și modul în care cancerul a răspuns la tratament. Este important să rețineți că prognosticul poate varia considerabil de la un pacient la altul.
Dacă operația de prostată a fost efectuată pentru tratarea cancerului de prostată, un factor semnificativ este dacă cancerul s-a răspândit în afara prostatei și dacă marginile chirurgicale au fost sau nu afectate de celulele canceroase. Stadiul exact al cancerului, determinat în timpul și după operație, va influența în mod direct prognosticul.
- Radioterapia- este a doua metodă de tratament folosită, putând fi utilizată ca prim tratament (în cazurile când cancerul este situat doar în interiorul prostatei ți este de grad scăzut, având aproximativ aceleași rezultate ca și prostatectomia radicală doar că într-un timp mai lung), ca parte a primului tratament în asociere cu tratamentul antihormonal (pentru cancerele care au spart capsula prostatica și au invadat țesuturile învecinate), ca tratament adjuvant (când cancerul nu a putut fi îndepărtat complet în urma intervenției chirurgicale), ca tratament de salvare (în cazul recurențelor dupa intervenția chirurgicală), în stadiile avansate (pentru a ajuta la menținerea cancerului sub control cât mai mult timp posibil și pentru a ajuta la prevenirea sau ameliorarea simptomelor), sau ca tratament paliativ (pentru ameliorarea simptomatologiei și îmbunătățirea calității vieții).
După radioterapie pentru cancerul de prostată, nivelul PSA (antigenul specific prostatic) poate experimenta anumite schimbări. Este important să înțelegem că valorile PSA pot varia în mod natural în timp, iar interpretarea lor corectă necesită luarea în considerare a mai multor factori. În general, următoarele informații pot oferi o perspectivă generală:
Perioada de după tratament : După radioterapie, valorile PSA pot rămâne ridicate sau pot crește inițial înainte de a începe să scadă. Acest fenomen, cunoscut sub numele de "rebond PSA," este obișnuit și poate fi observat în primele luni până la ani după tratament.Timpul după radioterapie : Valorile PSA pot continua să scadă treptat în lunile și anii care urmează radioterapiei. Scăderea nivelului PSA este un semn că tratamentul a fost eficient în controlul sau eliminarea celulelor canceroase.Nivelul stabilizat : După o perioadă de timp, nivelul PSA ar trebui să se stabilizeze la un anumit nivel sau să devină nedetectabil. Nivelurile nedetectabile indică faptul că PSA nu poate fi măsurat în sânge sau că este la un nivel foarte scăzut
De asemenea, există mai multe tipuri de iradiere:
A.Radioterapia cu fascicule externe(EBRT-external beam radiation therapy)-se administrează cu ajutorul unor acceleratoare liniare de particule ce emit fascicule de înaltă energie, cum ar fi razele X sau protoni și sunt direcționate către tumoră sau către focarele metastatice. Iradierea se administrează în ședințe zilnice ,5 zile/săptămână, pe o durată diferită poate merge până la 7-8 săptămâni în funcție de scopul iradierii. O ședință de tratament durează câteva minute 2-3 (VMAT), 8 minute (IMRT) și este nedureroasă.
Există mai multe tehnici de iradiere externă: 3D-CRT, IMRT, VMAT, SBRT.
Cu ajutorul acestor noi tehnici de iradiere, se pot administra doze mai mari de radiații și pot fi direcționate țintit asupra volumului țintă cu o toxicitate mult mai mică a organelor sănătoase din jur.
De asemenea, mai există și radioterapia externă cu fascicule de protoni.
Posibile efecte adverse ale radioterapiei externe:
- radiodermita (hiperpigmentarea tegumentului)
- diaree
- tenesme rectale+/vezicale (senzația de a face, dar fără a putea face)
- jet urinar mai slab, urinari mai frecvente
- incontinență urinară (mai rar ca în cazul chirurgiei)
- disurie (usturimi, durere la urinat)
- meteorism (balonare)
- fatigabilite (slăbiciune)
- lipsa poftei de mâncare
- reducerea numărului de celule sangvine
- disfuncții erectile/ impotență
- limfedem
Rezultatele la 10 ani de la finalizarea radioterapiei sunt similare cu cele obținute prin chirurgie, singura diferență făcând-o efectele secundare (radioterapia prezervă mai bine funcția sexuală și sfincteriană, însă pe termen lung există riscul pentru 2-4% din pacienți să dezvolte rectita radica (sângerare de la nivelul peretelui rectal) sau fistulă rectală.
B. Brahiterapia (numită și implantare de semințe sau radioterapie interstițială)- folosește pelete radioactive mici sau „semințe”, fiecare de dimensiunea unui bob de orez, ce sunt plasate direct în prostată. Aceasta poate fi utilizată fie singură (la pacienții în stadiul incipient și cu un grad scăzut), fie combinată cu EBRT (la cei cu risc mai mare de dezvoltare a cancerului în afara prostatei).
Utilizarea brahiterapiei este limitată de anumiți factori:
- TURP/pacienți cu probleme urinare -crește riscul de reacții adverse urinare.
- prostate cu dimensiuni mari-imposibilitatea de a plasa semințele în toate locațiile corecte.
Brahiterapie permanentă (LDR-low dose rate) și brahiterapie temporară (HDR-high dose rate).
Efectele adverse ale brahiterapiei:
- probleme intestinale (proctita radica, durerea rectală, arsuri și/sau diaree )
- probleme urinare (incontinență urinară, stricturi uretrale, disurie(usturimi la urinat))
- probleme cu funcția sexuală (funcția erectilă și ejacularea)
C. Radiofarmaceuticele (medicamente ce conțin elemente radioactive ce pot ucide celulele canceroase). Acestea sunt injectate într-o venă și prin sange pot ajunge la celulele canceroase care s-au răspândit în alte părți ale corpului. Au efecte adverse limitate întrucât pot călători pe o distanță scurtă.
Efecte adverse ale radiofarmaceuticelor:
- Oboseală
- Xerostomie (gură uscată)
- Greață și vărsături
- Pierderea apetitului
- Constipație
- Reducerea numărului de celule sangvine
- Afecțiuni renale
Crioterapia (numită și criochirurgie sau crioablație) este o metodă ce utilizează temperaturi foarte scăzute pentru a îngheța și a ucide celulele canceroase de prostată, precum și cea mai mare parte a prostatei. Se folosește în cazul recidivei cancerului după radioterapie sau în cazurile cu risc scăzut și în stadii incipiente ce nu pot beneficia de chirurgie sau radioterapie însă nu este folosită ca prim tratament în general. Deși este mai puțin invazivă decât intervenția chirurgicală, pacienții au mai puține pierderi de sânge, beneficiază de o perioadă de recuperare mai scurtă, spitalizare mai scurta și mai puțină durere, nu se cunoaște cu exactitate eficacitatea pe termen lung și nici nu poate fi o opțiune bună pentru pacienții cu prostate mari.
Efectele adverse posibile ale crioterapiei (sunt mai grave la pacienții care au facut deja radioterapie):
- inflamatia scrotului și penisului (frecvente)
- hematurie (sânge în urină), durere în zona în care au fost plasate acele (1-2 zile după procedură)
- durere, senzații de arsură și nevoia de a goli des vezica urinară și intestinele(se recuperează funcțiile în timp)
- disfuncția erectilă (mai frecventă decât în cazul chirurgiei)
- incontinența urinară (mai frecventă atunci când se face după radioterapie)
- fistula recto-vezicala(<1%)
Tratamentul cu ultrasunete focalizat de intensitate mare (HIFU) -Încălzește țesutul prostatic și determină necroza celulelor tumorale. Acest tratament este utilizat fie în cancerele de prostată foarte mici (în cazul în care nu e posibilă intervenția chirurgicală), fie în formele avansate de cancer ce nu au avut răspuns în urma altor tratamente precum radioterapia.
Terapia hormonală (terapie de supresie androgenică) are ca scop reducerea hormonilor masculini (androgeni)-(testosteronul si dihidrotestosteronul) și împiedicarea creșterii celulelor canceroase în prostată. Această terapie poate miscșora sau încetini procesul de creștere al cancerului de prostată însă nu poate vindeca singură. Este utilizată fie ca prim tratament în asociere cu radioterapia (scor Gleason mare, PSA mare și/sau creșterea cancerului în afara prostatei), fie ca prim tratament singur (pentru a micșora tumora și a face mai eficient tratamentul radioterapeutic), fie în cazul unei recidive (după tratamentul chirurgical sau radioterapeutic), fie în cazul în care cancerul s-a răspândit prea mult pentru a fi vindecat prin intervenție chirurgicală sau radioterapie sau în cazul în care pacientul nu poate urma aceste tratamente din alt motiv.
Terapia de privare de androgeni(ADT)-folosește intervenții chirurgicale sau medicamente pentru a scădea nivelul de androgeni produs de testicule.
Orhiectomie (castrare chirurgicală)-este ca o formă de terapie hormonală, întrucât chirurgul îndepărtează testiculele (locul unde se produc majoritatea androgenilor) și stopează creșterea tumorii sau chiar o micșorează.
Terapie cu agoniști sau antagoniști LHRH (medicamente care scad nivelurile hormonale- cantitatea de testosteron produsă de testicule).
Agoniștii LHRH - scad nivelurile de androgeni la fel de bine ca și orhiectomia însă în acest caz deși testiculele se vor micșora în timp, ele rămân pe loc. La prima administrare pot apărea efecte secundare precum dureri osoase, durere la nivelul coloanei vertebrale. O criză poate fi evitată prin administrarea de medicamente numite anti-androgeni timp de câteva săptămâni la începerea tratamentului cu agonişti LHRH.
Antagoniştii LHRH pot fi utilizaţi pentru a trata cancerul avansat de prostată. Aceștia scad nivelul de testosteron mai repede și nu provoacă apariția tumorii, așa cum o fac agoniștii LHRH.
Efectele adverse:
- scăderea sau dispariția apetitului sexual
- disfuncție erectilă (impotență)
- contracția testiculelor și a penisului
- bufeuri
- sensibilitatea sânilor și creșterea țesutului mamar (ginecomastie)
- osteoporoza (subțierea oaselor), care poate duce fracturi osoase
- anemie (număr scăzut de globule roșii)
- pierderea masei musculare
- creștere în greutate
- oboseală
- niveluri crescute de colesterol
- depresie
- probleme cu memoria/concentrarea
C.Tratament pentru scăderea nivelului de androgeni din alte părți ale corpului (celulele suprarenalele sau celulele canceroase din prostată)
Tratament cu anti-androgeni/antagoniști ai receptorilor de androgeni (medicamente care împiedică androgenii să funcționeze)
E. Anti-androgeni mai noi
Chimioterapia (utilizează medicamente anticancerigene ce se pot administra intravenos, sub forma unor pastile sau prin ambele modalități și pe calea fluxului sanguin ajung la celulele cancerigene din tot corpul). Aceasta este folosită în cazul pacienților cu cancer avansat care s-a răspândit și în alte zone ale corpului și nu mai răspunde la tratamentul antihormonal.
Efectele adverse posibile depind de tipul și doza de medicamente administrate și de cât timp sunt luate.
- pierderea părului
- afte bucale
- pierderea poftei de mâncare
- greață și vărsături
- diaree
- creșterea riscului de infecții (celule albe scăzute)
- vânătăi sau sângerări ușoare (trombocite scăzute)
- oboseală
- reacții alergice severe
- amorțeală, furnicături sau senzații de arsură la mâini sau picioare (neuropatie periferică)
Imunoterapia (utilizează medicamente ce stimulează propriul sistem imunitar să recunoască și să distrugă mai eficient celulele canceroase)
Vaccinul împotriva cancerului - întărește sistemul imunitar pentru a-l ajuta să atace celulele cancerului și este utilizat în formele avansate ce nu mai răspund la tratamentul hormonal cu sau fără simptome ușoare. Acest vaccin pare să prelungească supraviețuirea cu câteva luni însă nu există dovezi că ar vindeca cancerul.
Reacții adverse:
- febră
- frisoane
- oboseală
- dureri de spate și articulații
- greață și dureri de cap
- Terapia medicamentoasa țintită
indicată în cazurile de cancer avansat când acesta s-a răspândit în restul corpului la pacienții cu mutații genetice ale celulelor canceroase.
Inhibitori PARP-ajută în mod normal la repararea ADN-ului deteriorat din interiorul celulelor.
Se administrează sub formă de pastile de obicei de 2 ori pe zi și pot fi administrate împreună cu terapia hormonală sau după o orhiectomie.
Efectele adverse:
- greață,vărsături
- diaree
- oboseală
- pierderea poftei de mâncare
- anemie
- constipație
- erupții cutanate
- transaminaze hepatice anormale
- trombocite scazute
- tuse și dificultăți de respirație.
Efecte adverse rare
- sindromul mielodisplazic
- leucemia mieloidă acută.
- cheaguri de sânge în plămâni/picioare
Aceasta poate fi realizată prin adoptarea unui stil de viață sănătos (o dietă bogată în fructe și legume, evitarea grăsimilor nesănătoase, a zaharurilor, exerciții fizice regulate pentru menținerea unei greutăți normale), controale medicale periodice după vârsta de 50 de ani și screening-ul în cazul pacienților cu risc crescut, pentru depistarea precoce a eventualelor afecțiuni ce pot apărea la nivelul prostatei.
Indicatorii clinici de prognostic și șansele de vindecare țin de tipul histopatologic, de momentul diagnosticării, de stadiul bolii, de valoarea PSA-ului preterapie, de scorul Gleason, de starea generală de sănătate a pacientului, de vârstă și de reacția organismului la tratamentul administrat (cu cât scorul, stadiul și PSA-ul sunt mai mari cu atât prognosticul este mai slab).
În stadiile incipiente, rata de supraviețuire la 5 ani- 99%, 10 ani-98%, 15ani-96%.
Perioada post tratament pentru cancerul de prostată poate fi un moment crucial și necesită o abordare cuprinzătoare pentru a menține sănătatea generală și pentru a face față posibilelor efecte secundare ale tratamentelor. Iată câteva aspecte de luat în considerare în perioada post tratament:
Consultații regulate : După tratament, este important să continuați să vă vedeți medicul în mod regulat pentru examene de urmărire și teste necesare. Acest lucru poate implica teste PSA (antigenul specific prostatic), examinări fizice și alte teste specifice.Efecte secundare ale tratamentului : Tratamentele pentru cancerul de prostată pot avea diverse efecte secundare, cum ar fi probleme erectile, incontinență urinară sau alte probleme legate de funcția sexuală. Este important să discutați deschis cu medicul dumneavoastră despre orice efect secundar și să aflați despre opțiunile de gestionare disponibile.Reabilitare : În funcție de efectele secundare, puteți beneficia de programe de reabilitare, cum ar fi fizioterapia sau consilierea sexuală, pentru a vă ajuta să gestionați și să îmbunătățiți aspecte precum funcția erectilă sau controlul vezical.Activitatea fizică : Menținerea unui stil de viață activ poate avea beneficii semnificative pentru sănătatea generală și poate contribui la îmbunătățirea stării de bine.Alimentație sănătoasă : O dietă echilibrată și sănătoasă este esențială pentru menținerea unei greutăți sănătoase și pentru susținerea sistemului imunitar.Renunțarea la fumat : Dacă fumați, renunțarea la acest obicei poate avea un impact pozitiv asupra sănătății generale, inclusiv a sănătății prostatei.Consiliere psihologică : Tratamentul pentru cancer poate avea un impact emoțional semnificativ. Terapia sau consilierea psihologică poate fi benefică pentru a face față emoțiilor și pentru a vă ajuta să vă adaptați la schimbările survenite.Participarea la grupurile de suport : Participarea la grupuri de suport poate oferi o cale de comunicare cu alți oameni care trec prin aceeași experiență și poate fi un suport emoțional.
Locațiile noastre
Profesor Doctor Radioterapie
Medic Primar Oncologie Medicală
Șef Secție Radioterapie
Șef Secție Oncologie Medicală
